即可将网页分享至朋友圈
近日,电子科技大学生命科学与技术学院刘贻尧教授团队与陆军军医大学和法国图卢兹第三大学合作,在国际著名期刊《自然-通讯》(Nature Communications,影响因子:12.124)上发表题为“A biochemical network controlling basal myosin oscillation”(生物化学网络调控肌球蛋白振荡)的研究论文。刘贻尧教授团队青年教师秦翔博士为该文共同第一作者(排名第一),刘贻尧教授为论文联合通讯作者,电子科技大学生命科学与技术学院为共同第一作者单位和共同通讯单位。这是我校生命科学与技术学院在生物力学研究领域的重要突破。
该工作揭示了肌球蛋白振荡的正负反馈调节因子,提出Rho相关激酶(ROCK)的两种不同活化方式以及肌球蛋白磷酸酶参与了振荡的起始和终结,系统阐明了肌球蛋白的振荡机制。
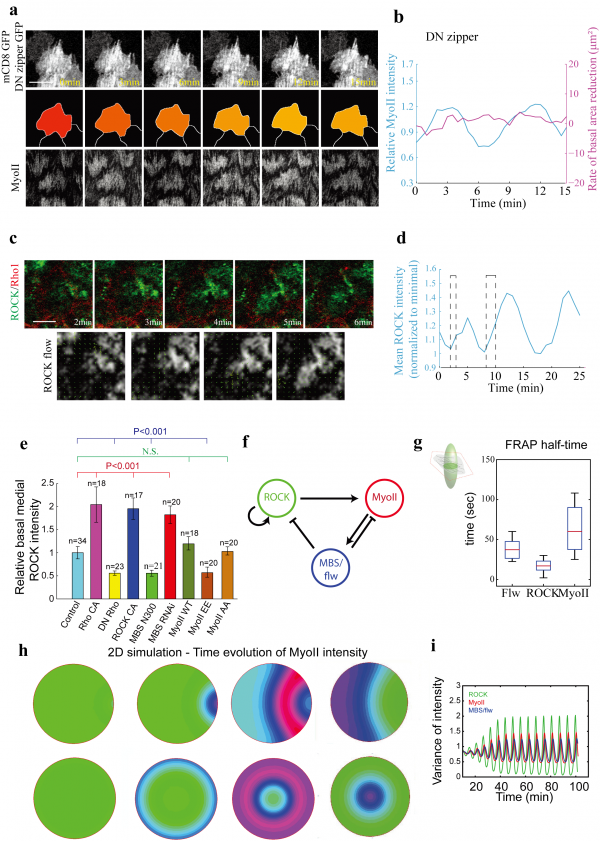
肌球蛋白振荡机制及其模拟。(a,b. 肌球蛋白振荡与细胞膜周期性变化的关系;c,d. ROCK与Rho结合导致其构象激活的转变;e-g. 揭示ROCK、肌球蛋白与肌球蛋白磷酸酶之间的相互关系;h,i. 肌球蛋白振荡的数学模拟). 图片修订自:(Qin et al. 2018, Nature Communications).
鉴于肌球蛋白在细胞骨架网络中的地位,阐明肌球蛋白的振荡机制将对亚细胞和分子蛋白水平的细胞骨架动力学研究具有重要意义。肌球蛋白收缩产生的生物力对于组织形成和内环境的稳态是必不可少的参与因素,但由于目前缺少有效的检测手段,探究力的产生和传导以及力与组织的整合极具挑战性。肌球蛋白作为与细胞骨架密切相关的动力蛋白,对其振荡的起源学术界也持有不同观点。
该研究证实了力学因素不是肌球蛋白振荡的起源,但肌球蛋白振荡介导的生物力直接调控了细胞周期性的形态变化。文章通过“空间-时间图像相关光谱分析”以及信号强度分析,揭示了由ROCK、肌球蛋白和肌球蛋白磷酸酶组成的生化振荡正负调控是肌球蛋白振荡的起源与终止因素。ROCK的激活是从与Rho相互作用打开构象开始,进而通过寡聚化放大ROCK信号,放大的信号招募了肌球蛋白磷酸酶的重新定位,最终通过负反馈ROCK信号影响了肌球蛋白磷酸化。该研究清晰展示出肌球蛋白振荡的全过程,对细胞骨架动力学的发展具有重要意义。
秦翔,博士,生命科学与技术学院讲师。先后在四川农业大学、重庆大学和法国图卢兹第三大学,获得学士、硕士和博士学位,主要从事细胞骨架动力学与光遗传学等相关交叉学科的研究。迄今已在Nature Communications(第一作者2篇)、ACS Applied Materials & Interfaces、Biochimica et Biophysica Acta(BBA)-Molecular Cell Research等发表SCI收录论文8篇。先后获得国家建设高水平大学公派研究生奖学金、法国癌症预防基金会奖学金等,参加国家自然科学基金、法国国家研究署等多项研究工作。
刘贻尧,生命科学与技术学院教授。2004年毕业于日本群马大学,获博士学位;2005-2007年在日本德岛大学医学部做博士后研究;2008年晋升教授、博士生导师。长期从事细胞力学、力学生物学及微纳医学等相关交叉学科的研究,近年来主持了包括国家自然科学基金等课题10余项。迄今已在Nature Communications、Biotechnology Advances、Journal of Controlled Release、ACS Applied Materials & Interfaces、Acta Biomaterialia、Cancer Letter、International Journal of Cancer、Molecular & Cellular Immunology等发表SCI收录论文70余篇,SCI他引1000余次。先后入选教育部新世纪优秀人才计划、四川省有突出贡献的专家、四川省学术技术带头人,获四川省杰出青年基金。
《Nature Communications》是《Nature》出版集团于2010年发行的子刊,综合性一区著名期刊,收录了各研究领域前沿优秀论文,2017年影响因子为12.124。《Nature Communications》主要发布严谨而颇具综合性并代表某一领域主要进展的研究论文,其文章类型涉及生命科学、物理学、化学、地球科学等,旨在传播一流的、最新的科学研究成果。
论文链接:
https://www.nature.com/articles/s41467-018-03574-5
编辑:林坤 / 审核:罗莎 / 发布:陈伟


